 您的购物车当前为空
您的购物车当前为空
下一代CDK4/6抑制剂——Atirmociclib有什么特点?

异常细胞增殖是人类癌症的基本特征之一。在肿瘤细胞中,细胞周期蛋白 D 依赖性激酶 CDK4 和 CDK6 共同驱动着细胞异常增殖,尤其在HR+乳腺癌中,CDK4 的活性对细胞周期 G1-S 期转换至关重要。
基于CDK4/6在癌症中的作用,CDK4/6抑制剂 帕博西尼( palbociclib ) 、瑞博西尼( ribociclib ) 和阿贝西利( abemaciclib ) 被成功开发,并成为HR+ HER2− 乳腺癌的一线治疗方案。
从毒性角度来看,中性粒细胞减少是帕博西尼和瑞博西尼最常见的不良反应,同时也是阿西贝利的第二大不良反应。阿贝西利的毒性特征较为独特,其主要不良反应为胃肠道不适和腹泻,这主要归因于其多靶点作用,额外抑制 CDK9 和 GSK3β,从而影响肠道隐窝细胞增殖。
虽然这些抑制剂均可同时抑制CDK4和CDK6,但在CDK4和CDK6的抑制比率上略有不同。帕博西尼 1:1.5,瑞博西尼 1:4,阿贝西利 1:5。此外,在临床相关剂量下,帕博西尼和阿贝西利对 CDK4 的抑制作用更强,而对 CDK6 的抑制受限于其相关的血液学毒性。
因此,有研究认为提高 CDK4 选择性抑制,可在降低 CDK6 相关毒性的同时改善CDK抑制剂的安全性和疗效。例如3月18日以CDK4 selective inhibition improves preclinical anti-tumor efficacy and safety为题发表于 Cancer Cell 期刊的一篇研究性论文。

该研究先是探讨了肿瘤和造血系统中CDK4和CDK6的不同作用依赖性。
通过对DepMap数据进行分析,发现依赖 CDK4 的肿瘤类型(如 HR+ 乳腺癌、转移性前列腺癌和尤文氏肉瘤)对 CDK6 依赖性较低或几乎没有依赖,同时,这些肿瘤类型也高度依赖细胞周期蛋白 D1(cyclin D1)。而CDK6 的低表达与肿瘤细胞对 CDK4 的依赖性呈负相关。这些结果表明,HR+ 乳腺癌、尤文氏肉瘤和前列腺癌细胞对 CDK4 的依赖性可通过 CDK6 低表达和 cyclin D1 高表达状态进行预测。
在造血系统方面,研究发现单独去除 CDK4 对骨髓来源的细胞没有显著影响,但去除 CDK4 和 CDK6 时,细胞数目显著减少,单独去除 CDK6 的效果较轻。这与CDK4 在某些肿瘤类型中的严格依赖性形成鲜明对比。
CDK4/6 在不同细胞中的蛋白质表达比率也存在显著差异。HR+ 乳腺癌和前列腺癌细胞中 CDK4 的高表达与 CDK6 的低表达密切相关,而在骨髓来源的细胞中则恰恰相反。
基于这些发现,研究提出,CDK6 抑制可能会对依赖 CDK4 的肿瘤(如 HR+ HER2− 乳腺癌)产生潜在的不利影响。研究还提出,当前临床使用的双重 CDK4/6 抑制剂可能并不是治疗高度依赖 CDK4 的肿瘤的最佳选择,开发具有更高选择性的 CDK4 抑制剂可能会为这些肿瘤类型提供显著的治疗优势。

研究示意图
因此,研究者开始着手筛选具有更高 CDK4 选择性的新一代抑制剂,发现了 atirmociclib(PF-07220060)。
Atirmociclib 的选择性
Atirmociclib 在与 CDK4 和 CDK6 的结合中存在结构差异,特别是在两者的甘氨酸富含环(G-loop)区域。
CDK6 的 G-loop 由于盐桥的稳定作用,使得抑制剂的异丙醇基团难以进入,而 CDK4 的 G-loop 更为灵活,从而使 atirmociclib 更易与 CDK4 结合,这种结构上的差异可能是其选择性偏向 CDK4 的原因。
在细胞实验中,Atirmociclib 在 HR+ 乳腺癌细胞中具有与 palbociclib 相似的抗增殖能力,但对造血干/祖细胞(CD34+ HSPC)和骨髓细胞的影响明显降低。
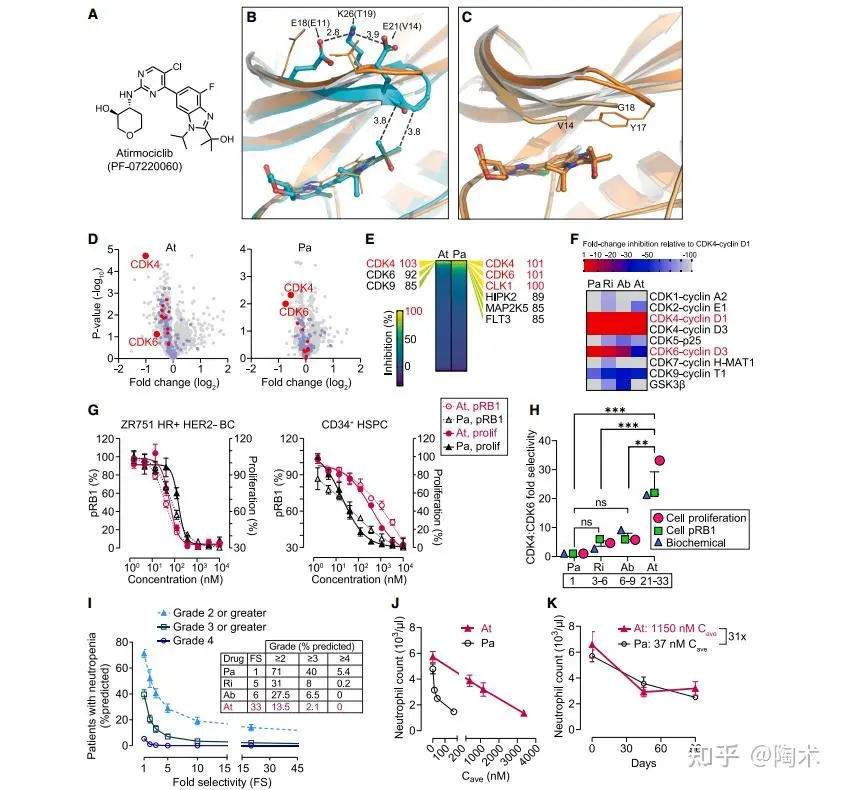
▲atirmociclib 利用 CDK4/6 G 环的构象差异,相比 palbociclib 在体外对 CD34+ 造血干/祖细胞(HSPC)的影响降低约 30 倍,在体内对中性粒细胞的影响亦显著降低。
Atirmociclib 的抗肿瘤活性
Atirmociclib 在 3D 肿瘤球(spheroids)和多种小鼠异种移植(xenograft)模型中表现出强大的抗肿瘤作用。相比于 palbociclib,Atirmociclib 在 HR+ 乳腺癌、前列腺癌和 Ewing 肉瘤模型中显示出更深度的肿瘤抑制效果(TGI),且其作用与 CDK4 靶点覆盖度直接相关。
进一步研究表明,Atirmociclib 能有效抑制视网膜母细胞瘤蛋白(pRB1 )的磷酸化,这是 CDK4/6 作用于 G1-S 期转变的关键底物。此外,在 HR+ 乳腺癌异种移植模型中,Atirmociclib 单药治疗的肿瘤生长抑制效果优于 palbociclib,并且在前列腺癌模型中,其单药治疗效果甚至优于 palbociclib 联合雄激素受体(AR)抑制剂 enzalutamide 的疗效。

▲增加 CDK4 覆盖可显著抑制多细胞肿瘤类器官和 cyclin D1-CDK4 通路激活的肿瘤模型的生长
Atirmociclib 可能的耐药机制
尽管 Atirmociclib 显示出卓越的抗肿瘤活性,但部分肿瘤细胞仍可能通过耐药机制逃逸治疗。
研究发现,在部分 HR+ 乳腺癌细胞中,CDK6 表达上调可能会降低 Atirmociclib 的敏感性,但这一现象发生率较低。此外,RNA 测序和信号通路分析显示,耐药肿瘤可能通过以下途径获得逃逸能力:
1.Cyclin E1-CDK2 轴激活:
耐药肿瘤中 Cyclin E1(CCNE1)显著上调,促进 CDK2 介导的细胞周期进程。
2.雌激素受体(ER)信号增强:
耐药肿瘤中 ER 相关基因上调,表明 ER 可能成为逃逸 CDK4 抑制的重要途径。
3.TNF-α/NF-κB 信号通路激活:
耐药肿瘤表现出 TNF-α 依赖的 NF-κB 活化,可能促进肿瘤细胞存活和增殖。
针对这些耐药机制,研究者进一步探索了 Atirmociclib 在联合治疗中的潜力。
1. Atirmociclib + 内分泌治疗(ET)
Atirmociclib 与 Fulvestrant(ER 降解剂)联用,在 HR+ HER2- 乳腺癌中显示出协同作用。联合治疗可显著增强 G1 期阻滞并诱导肿瘤细胞衰老(senescence),从而实现长期肿瘤生长控制。此外,与 ER 降解剂 PROTAC(如 ARV-471)联用可进一步延缓肿瘤复发。
2. Atirmociclib + CDK2 抑制剂
由于 Cyclin E1-CDK2 介导的耐药性,Atirmociclib 与 CDK2 选择性抑制剂(PF-07104091)联合可增强抗肿瘤效果。在 HR+ HER2- 乳腺癌模型中,该组合可显著降低 pRB1 和 FOXM1 的表达,并诱导更强的细胞周期停滞,显示出较单药治疗更好的疗效。
3. Atirmociclib + HER2 靶向治疗
Atirmociclib 处理后,HER2- 乳腺癌细胞表面 HER2 表达显著上调,提示其可作为 HER2 靶向治疗的增敏剂。实验表明,Atirmociclib 与 HER2 单抗(Trastuzumab )或 HER2-ADC(如 PF-06804113)联合使用,可有效增强肿瘤抑制效果。
4. Atirmociclib + 免疫检查点抑制剂(ICI) :
Atirmociclib 可通过增强抗原呈递和干扰素信号,提高肿瘤免疫可识别性,从而提高 PD-1/PD-L1 免疫治疗的效果。在小鼠 MC38R 和 CT26 同基因移植模型中,Atirmociclib 与 PD-1 抑制剂 联用可显著抑制肿瘤生长,优于 palbociclib 组合治疗的效果。
小结:
Atirmociclib 作为新一代 CDK4 选择性抑制剂,在 HR+ HER2- 乳腺癌和其他 CDK4 依赖型癌症中展现了卓越的抗肿瘤活性,并且相比现有的 CDK4/6 抑制剂,具有更低的血液学毒性。其与 ET、CDK2 抑制剂、HER2 抗体及 ICI 组合使用,可有效克服耐药性,并扩大细胞周期抑制剂的应用范围。目前,Atirmociclib 正在多个临床试验(如 NCT04557449、NCT061056320 和 NCT05262400)中进行评估,未来有望成为 HR+ HER2- 乳腺癌及其他 CDK4 依赖性肿瘤的新型治疗选择。
TargetMol可提供多种CDK4/6抑制剂,以及抗乳腺癌化合物库 ,助力相关研究。
乳腺癌是乳腺恶性肿瘤,是全球女性发病率较高的癌症,约占女性癌症患者的20%,也是100多个国家癌症死亡的主要原因。近年来全球乳腺癌发病率一直呈上升趋势。 乳腺癌根据病理分型可分为非浸润性癌,早期浸润性癌,浸润性癌。根据分子分型可分为雌激素受体阳性乳腺癌(ER+PR+HER2-),HER2阳性乳腺癌(ER-PR-HER2+),三阴性乳腺癌(ER-PR-HER2-)。
不同类型的乳腺癌,从治疗方法到预后都是非常不同,需要针对已经明确的致癌位点,探索相关靶点来设计相应的药物。 TargetMol 抗乳腺癌库 收集了2440 种与乳腺癌相关的化合物,包含了已经报道的有乳腺癌治疗作用的化合物,以及相关的靶点通路(HER-2, VEGF, EGFR, PARP, CDK4/6, HSP, PD-1, SET7/9, BRCA 等),是乳腺癌药物研发的良好工具。

原文链接:
https://www.cell.com/cancer-cell/fulltext/S1535-6108(25)00058-3#sec-2
其他文章


订阅TargetMol新闻
科学新闻、观点和分析的重要汇总,每个工作日都会发送到您的收件箱.




 |
|