- 全部删除
 您的购物车当前为空
您的购物车当前为空

- 具有直观的搜索结果
- 更便捷高效地比较产品细节
- 快速、简洁的提交订单
- 成为我们TargetMol的一员,阅读和提交您的产品建议和意见
我们很想知道您的意见反馈,所以我们在每个页面上都梳理出一个反馈按钮。

药物开发计划的启动,是因为有一种疾病或临床状况没有合适的医疗产品可用,这种未满足的临床需求正是该计划的潜在驱动因素。而在开发新药物的过程中,最重要的步骤之一是确定和验证药物的靶点。
这里的靶点是一个广义的术语,囊括了蛋白质、基因、RNA等。一个好的靶点需要具有疗效、安全性、满足临床和商业需求,最重要的是“可成药”。
靶点发现
靶点的确定主要基于生物医学数据的可用性。可用的数据来自各种来源,包括出版物、专利信息、基因表达数据、蛋白质组学数据、转基因表型以及化合物筛选数据等等。
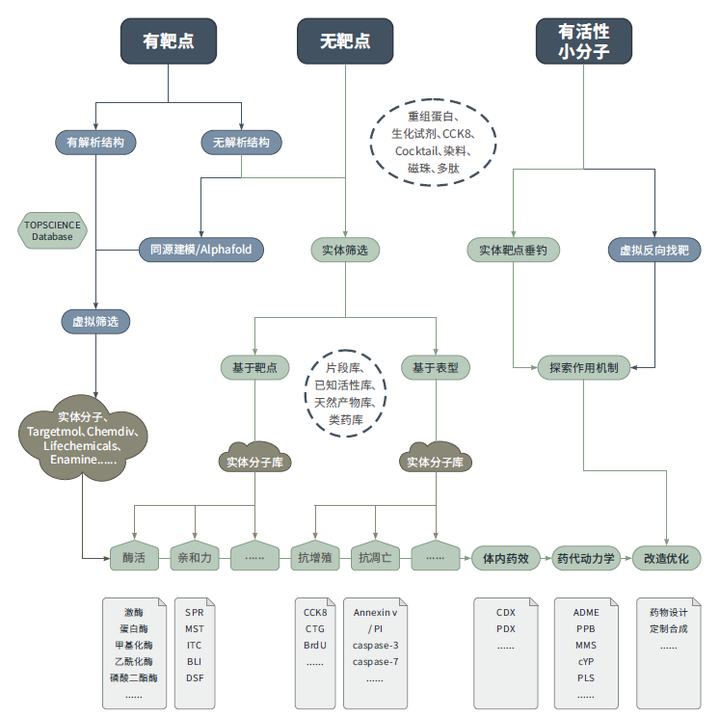
1.基于靶点结构的药物筛选方案
若有明确的靶点蛋⽩,且结构已被解析或可通过 Alphafold 预测获得,找到合适的对接位点,即可开展虚拟筛选。
常规虚筛数据量在百万级别,对海量化合物和靶点的亲和程度进⾏打分排序,由此选出 TOP100-200 个化合物进⼊实体验证环节。实体验证环节⼀般包含两个⽅⾯,即亲和⼒检测和功能检测。⽣物物理⽅法检测亲和⼒有多种技术可选, SPR /MST / BLI / ITC / DSF 等均可达到⽬的。功能检测主要依据研究⽅向和治疗⽬的来确定,可依次选择分⼦⽔平、细胞⽔平、动物⽔平的检测层层筛选,最终获得在体内外均具有良好效果的苗头化合物。
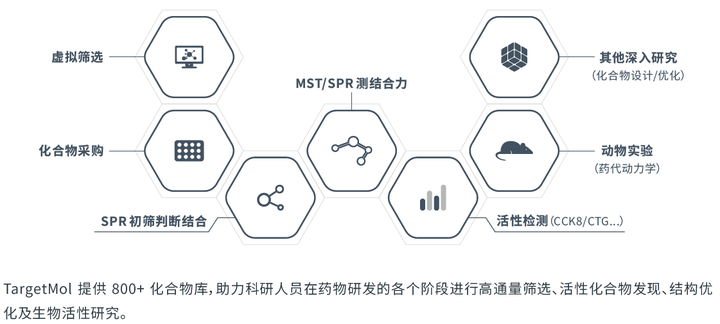
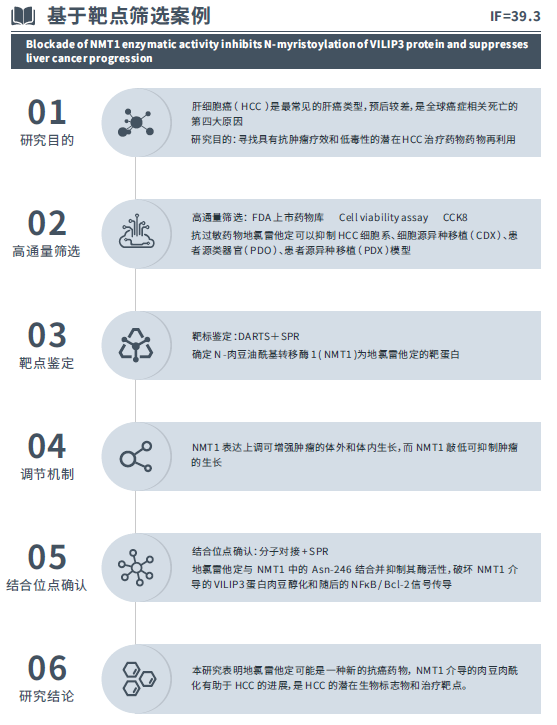
2.基于表型的药物筛选方案
若未明确药物靶点,可以选择从表型⼊⼿筛选有效化合物。基于表型的药物筛选是以拟设计药物作⽤的靶细胞作为研究对象,这是更接近⽣理条件的药物筛选模型。应⽤细胞培养技术获取所需细胞,将这些细胞与候选化合物相互作⽤,通过显微镜或酶标仪收集产⽣的信号评估化合物的作⽤效果,从⽽对化合物进⾏筛选。
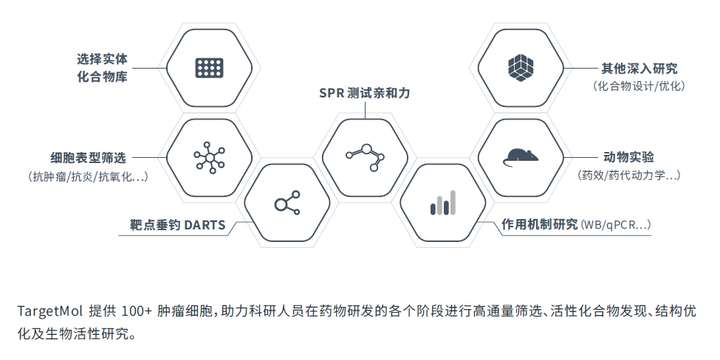

DARTS 技术
DARTS( Drug Affinity Responsive Target Stability ) 是根据⼩分⼦药物与其靶标蛋⽩结合后导致靶蛋⽩对蛋⽩酶降解的敏感性下降⽽发展起来的⼀项新技术,由于⽆需药物保护性修饰且⽆药物活性依赖性,可⼴泛应⽤于药物筛选与靶标鉴定。DARTS 实验需要⽤特定的⽅法对酶解效果进⾏检测,常⽤的⽅法有 SDS-PAGE 、胶染⾊技术(如考⻢斯亮蓝染⾊)等,此外也可以运⽤蛋⽩⼆维电泳( 2D-PAGE )、凝胶或⾮凝胶质谱( LC-MS/MS )等⽅法进⾏检测。通过⽐对,识别药物组与对照组酶解的明显差异,进⽽找到药物的候选靶点进⾏后续实验确证。
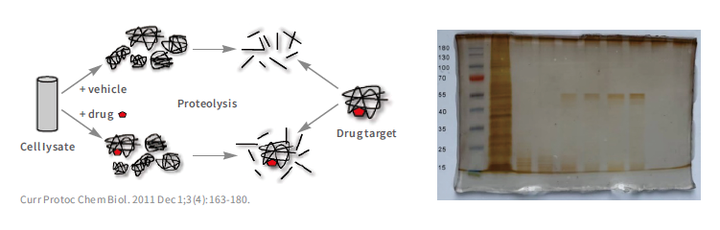
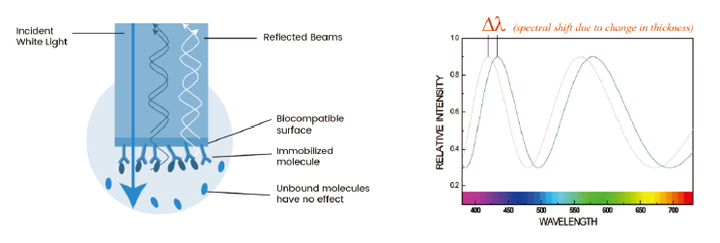
BLI 垂钓
⽣物膜层⼲涉技术(BLI),将⽣物分⼦ A 结合到光纤材质的⽣物传感器末端会形成⼀层⽣物膜,当传感器末端的分⼦ A 与待检测分⼦ B 结合时会引起传感器末端分⼦量的改变,从⽽导致⽣物膜厚度的改变。光通过传感器的⽣物膜层后发⽣透射和反射形成⼲涉光波,⽣物膜厚度的变化导致⼲涉光波发⽣相对位移。⽣物分⼦结合前后的⼲涉光波被光谱仪检测到,形成⼲涉光谱,以⼲涉图谱的实时位移( nm )显⽰出来。最后根据分⼦结合前后图谱的变化对待检测分⼦进⾏分析。通过 BLI 技术垂钓到与 Compound X 有结合的⽬标蛋⽩,洗脱下来进⾏质谱检测,分析数据获得靶蛋⽩。
激酶谱筛选
蛋⽩激酶是药物研发领域重要的药靶之⼀,激酶功能的失调与许多疾病的发⽣发展密切相关,涉及⼈类的各种细胞信号传导途径,通过磷酸化其各⾃的下游特定底物蛋⽩来发挥其作⽤。激酶介导的信号传导途径的异常调节是造成主要⼈类病理状况的原因,例如癌症、⾃⾝免疫性疾病、⼼⾎管疾病、神经退⾏性疾病和代谢紊乱等。⽬前已鉴定的激酶超过500种,包括⼗个家族: TK, STE,TKL, AGC, CMGC, CAMK,RGC, CK1, Atypical ,other。
TargetMol提供:
- 超过 400 种激酶靶点的化合物筛选模型及激酶谱筛选;
- 充⾜的筛选资源,提供多种筛选化合物库和抑制剂;
- ⾼通量筛选,可以筛选数以万计的化合物规模;
- 实验灵活,可以开展 96 和 384 等多种板型的筛选实验;
- 严格保证客⼾信息安全,TargetMol 将严格按照与客⼾签订的保密合同执⾏服务。
根据确定的靶点或表型以及经费情况选择合适的筛选策略。 TargetMol 为⼴⼤药物研发客⼾提供种类丰富的筛选化合物库、重组蛋⽩、试剂盒、以及专业的技术服务,轻松获得实现药物发现⼀站式解决⽅案。
⽬前提供的化合物活性筛选服务已覆盖⼤部分重要靶点,包括酶学靶点、 G 蛋⽩偶联受体(GPCRs )、离⼦通道以及核受体等多项靶点筛选服务和抗肿瘤药物体外筛选服务。 TargetMol 专业的筛选平台能够帮助您判断化合物是否进⼊下⼀阶段的开发流程,为您的药物研发节约宝贵的时间和经费。
靶点验证
一旦确定目标,接下来需要对其进行全面的验证。验证技术多种多样,虽然每种方法都是有效的,但通过多重验证的方法可以大幅增加对观察结果的信心。
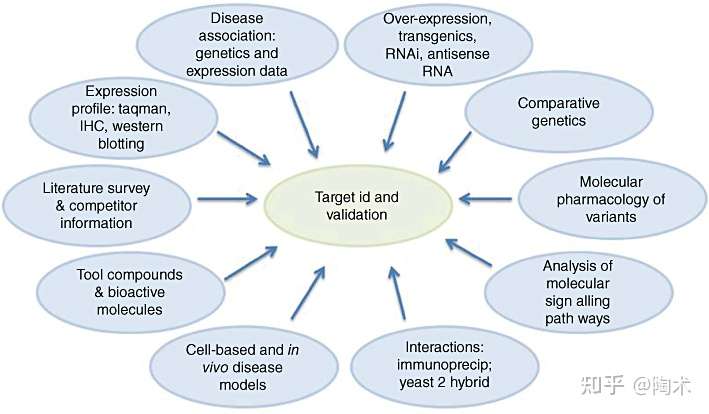
靶点验证
常见的方法如下:
反义技术
反义技术利用反义寡核苷酸(antisense oligonucleotides)或反义RNA(antisense RNA)来调控或抑制特定基因的表达。这种技术的基本原理是通过合成与目标基因的mRNA序列互补的反义寡核苷酸或反义RNA,从而干扰或阻止目标基因的翻译过程,使其不被转录成蛋白质。
转基因动物
转基因动物是指在其基因组中插入外源DNA的动物。这些外源DNA通常是与特定基因相关的DNA序列,可以用来研究该基因的功能。转基因动物可以通过多种方法创建,包括基因敲除、基因敲入和基因突变,是研究基因功能和疾病机制的重要工具。
siRNA靶标验证
siRNA靶标验证是一种利用小干扰RNA(siRNA)来验证潜在药物靶点的技术。在这种技术中,双链RNA(dsRNA)特异性地靶向要沉默的基因被引入到细胞或生物体中,被识别为外源遗传物质并激活RNA干扰(RNAi)途径。核酸酶蛋白Dicer被激活,结合并切割dsRNA,产生21-25个碱基对的双链片段,其中有一些未配对的悬垂末端。这些siRNA片段与靶向mRNA结合,导致其降解,从而抑制目标基因的表达。通过观察siRNA沉默后的表型,可以验证潜在药物靶点的功能。
单克隆抗体
单克隆抗体是一种极好的靶标验证工具,因为它们与靶分子表面的更大区域相互作用,甚至可以更好地区分密切相关的靶标,并且通常提供更高的亲和力。相比之下,小分子由于需要与靶标通常更保守的活性位点相互作用而处于不利地位,而可以选择抗体与独特的表位结合。这种精湛的特异性是它们缺乏非机械(或“脱靶”)毒性的基础——这是与小分子药物相比的主要优势。
化学基因组学
化学基因组学是一种系统应用工具分子进行靶标识别和验证的方法。可以定义为对化合物对基因组的反应的研究。其目标是快速识别新药物和药物靶点,包括从靶点识别和验证、化合物设计和化学合成到生物测试的多个早期药物发现技术。该方法的最终目标是提供针对基因组编码的每个蛋白质的化学工具。其目的是在对靶点进行全面投资和筛选活动之前,使用这些工具来评估细胞功能。
亲和力测试
在⽣命科学领域中,研究⽣物分⼦间的相互作⽤对于阐明细胞⽣物学事件、揭⽰疾病发⽣机制以及药物发现都具有重要意义。“有结合才会有功能,有功能⼀定有结合”,结合是候选药物发挥功能的必要条件。⼩分⼦⼀直是分⼦互作研究的热⻔对象,例如化药、中药、植物激素、⾦属离⼦等。 TargetMol 提供多种体外评价⼩分⼦药物与靶标蛋⽩结合的技术服务,包括 SPR( 表⾯等离⼦体共振技术 )、 MST( 微量热泳动技术 )、 BL(I ⽣物膜⼲涉技术 )、ITC( 等温滴定量热法 )、 DSF( 差⽰扫描荧光法 )等。
药代动力学检测
临床前药代动⼒学( Pharmacokinetics, PK )研究是通过整体动物或体外试验以及虚拟仿真等研究⽅法,揭⽰药物在体内的动态变化规律,获得药物的基本药代动⼒学参数,阐明药物的吸收、分布、代谢和排泄( Absorption,Distribution, Metabolism, Excretion, 简称 ADME )的过程和特征。药代动⼒学研究在新药研究开发的评价过程中起着重要作⽤,对于预测药物的⽣物利⽤度和⽣物活性具有重要的参考价值。
所以在临床开发之前进行更多的研究,如改进的毒理学筛选(利用失败的药物来指导这些检测),建立基于深入了解疾病的预测性转化模型,以及确定生物标志物等可能有助于在临床前阶段增加药物价值,并最终有助于将更有效的药物带给患者。
参考文献
1. Xiao, Meng-Chao et al. “TRIB3-TRIM8 complex drives NAFLD progression by regulating HNF4αstability.” Journal of hepatology vol. 80,5 (2024): 778-791. doi:10.1016/j.jhep.2023.12.029
2. Yong, Liang et al.“ Calcium/calmodulin-dependent protein kinase IV promotes imiquimod-inducedpsoriatic inflammation via macrophages and keratinocytes in mice.” Nature communications vol. 13,14255. 22 Jul. 2022, doi:10.1038/s41467-022-31935-8
3. Yu, Yafen et al. “Cutaneous Calcium/Calmodulin-Dependent Protein Kinase II-γ-PositiveSympathetic Nerves Secreting Norepinephrine Dictate Psoriasis.” Advanced science (Weinheim,Baden-Wurttemberg, Germany) vol. 11,23 (2024): e2306772. doi:10.1002/advs.202306772
4. Deng, Ping et al.“ SIRT5-Mediated Desuccinylation of RAB7A Protects Against Cadmium-InducedAlzheimer's Disease-Like Pathology by Restoring Autophagic Flux.” Advanced science (Weinheim,Baden-Wurttemberg, Germany), e2402030. 5 Jun. 2024, doi:10.1002/advs.202402030
5. Bai, Yu-Bin et al.“ Virtual Screening and In Vitro Experimental Verification of LuxS Inhibitors forE s c h e r i c h i a c o l i O 1 5 7 : H 7 .” M i c r o b i o l o g y s p e c t r u m , v o l . 1 1 , 2 e 0 3 5 0 2 2 2 . 2 1 F e b . 2 0 2 3 ,doi:10.1128/spectrum.03502-22
6. Liu, Juan et al.“ Computational Drug Repurposing Approach to Identify Novel Inhibitors of ILKProtein for Treatment of Esophageal Squamous Cell Carcinoma.” Journal of oncology vol. 20223658334. 29 Dec. 2022, doi:10.1155/2022/3658334
7. Li J, Zheng C, Mai Q, Huang X, Pan W, Lu J, Chen Z, Zhang S, Zhang C, Huang H, Chen Y, Guo H, Wu Z,Deng C, Jiang Y, Li B, Liu J, Yao S, Pan C. Tyrosine catabolism enhances genotoxic chemotherapy bysuppressing translesion DNA synthesis in epithelial ovarian cancer. Cell Metab. 2023 Nov 7;35(11):2044-2059.e8.
8. Shi W, Zhang G, Ma Z, Li L, Liu M, Qin L, Yu Z, Zhao L, Liu Y, Zhang X, Qin J, Ye H, Jiang X, Zhou H, SunH, Jiao Z. Hyperactivation of HER2-SHCBP1-PLK1 axis promotes tumor cell mitosis and impairstrastuzumab sensitivity to gastric cancer. Nat Commun. 2021 May 14;12(1):2812.
9. Yang Y, Sun N, Lv J, Chen H, Wang H, Xu J, Hu J, Tao L, Fang M, Huang Y. Environmentally realisticdose of tire-derived metabolite 6PPD-Q exposure causes intestinal jejunum and ileum damage in micevia cannabinoid receptor-activated inflammation. Sci Total Environ. 2024 Mar 25;918:170679.
10. Hong X, Wei Z, He L, Bu Q, Wu G, Chen G, He W, Deng Q, Huang S, Huang Y, Yu C, Luo X, Lin Y. Highthroughputvirtual screening to identify potential small molecule inhibitors of the Zα domain of theadenosine deaminases acting on RNA 1(ADAR1). Eur J Pharm Sci. 2024 Feb 1;193:106672.
11. Du J, Liu N, Ma L, Liu R, Zuo D, Lan X, Yang J, Wei W, Peng X, Yu J. Antidepressant effect of the novelhistone deacetylase -5 inhibitor T2943 in a chronic restraint stress mouse model. BiomedPharmacother. 2024 Feb;171:116176.
12. Chen Y, Li L, Lan J, Cui Y, Rao X, Zhao J, Xing T, Ju G, Song G, Lou J, Liang J. CRISPR screens uncoverprotective effect of PSTK as a regulator of chemotherapy-induced ferroptosis in hepatocellular
carcinoma. Mol Cancer. 2022 Jan 4;21(1):11.
13. Xie Y, Zhang L, Wang L, Chen B, Guo X, Yang Y, Shi W, Chen A, Yi J, Tang J, Xiang J. EphB1 promotesthe differentiation and maturation of dendritic cells in non-small cell lung cancer. Cancer Lett. 2024 Feb1;582:216567
14. Yu Z, Peng Y, Gao J, Zhou M, Shi L, Zhao F, Wang C, Tian X, Feng L, Huo X, Zhang B, Liu M, Fang D, MaX. The p23 co-chaperone is a succinate-activated COX-2 transcription factor in lung adenocarcinomatumorigenesis. Sci Adv. 2023 Jun 30;9(26):eade0387. doi: 10.1126/sciadv.ade0387. Epub 2023 Jun 30.
15. Bai YB, Yang XR, Li B, Zhou XZ, Wang WW, Cheng FS, Zhang JY. Virtual Screening and In VitroExperimental Verification of LuxS Inhibitors for Escherichia coli O157:H7. Microbiol Spectr. 2023 Feb21;11(2):e0350222.
16. Wang J, Ran T, Chen Y, Lu T. Bayesian machine learning to discover Bruton's tyrosine kinaseinhibitors. Chem Biol Drug Des. 2020 Oct;96(4):1114-1122.
17. Wang W, Liu C, Li H, Tian S, Liu Y, Wang N, Yan D, Li H, Hu Q. Discovery of novel and potent P2Y14Rantagonists via structure-based virtual screening for the treatment of acute gouty arthritis. J Adv Res.2020 Feb 13;23:133-142.
18. Hughes JP, Rees S, Kalindjian SB, Philpott KL. Principles of early drug discovery. Br J Pharmacol. 2011;162(6):1239-1249. doi:10.1111/j.1476-5381.2010.01127.x
19. Kurosawa G, Akahori Y, Morita M, Sumitomo M, Sato N,Muramatsu C et al. (2008). Comprehensive screening for antigens overexpressed on carcinomas via isolation of human mAbs that may be therapeutic. Proc Natl Acad Sci U S A 105: 7287–7292
其他文章


订阅TargetMol新闻
科学新闻、观点和分析的重要汇总,每个工作日都会发送到您的收件箱.

 嗨!很高兴为您提供帮助!
嗨!很高兴为您提供帮助!










